Κλινικές δοκιμές έχουν επιβεβαιώσει ότι υψηλότερες δόσειςΣεμαγλουτίδημπορούν να βοηθήσουν με ασφάλεια και αποτελεσματικότητα τους ενήλικες με παχυσαρκία να επιτύχουν σημαντική μείωση βάρους. Αυτό το εύρημα προσφέρει μια νέα θεραπευτική προσέγγιση στην αυξανόμενη παγκόσμια επιδημία παχυσαρκίας.
Φόντο
Η σεμαγλουτίδη είναι ένααγωνιστής υποδοχέα GLP-1αρχικά αναπτύχθηκε για τον έλεγχο της γλυκόζης στο αίμα στον διαβήτη τύπου 2. Τα τελευταία χρόνια, οι ερευνητές έχουν ανακαλύψει τον αξιοσημείωτο ρόλο του στηνρύθμιση της όρεξης και διαχείριση βάρουςΜιμούμενη τη δράση του GLP-1, η σεμαγλουτίδη μειώνει την όρεξη και καθυστερεί την γαστρική κένωση, μειώνοντας τελικά την πρόσληψη τροφής.
Κλινικά δεδομένα
Ο παρακάτω πίνακας συνοψίζει τα αποτελέσματα απώλειας βάρους που παρατηρήθηκαν με διαφορετικές δόσεις Σεμαγλουτίδης σε κλινικές δοκιμές:
| Δόση (mg/εβδομάδα) | Μέση Μείωση Βάρους (%) | Συμμετέχοντες (n) |
|---|---|---|
| 1.0 | 6% | 300 |
| 2.4 | 12% | 500 |
| 5.0 | 15% | 450 |
Ανάλυση Δεδομένων
-
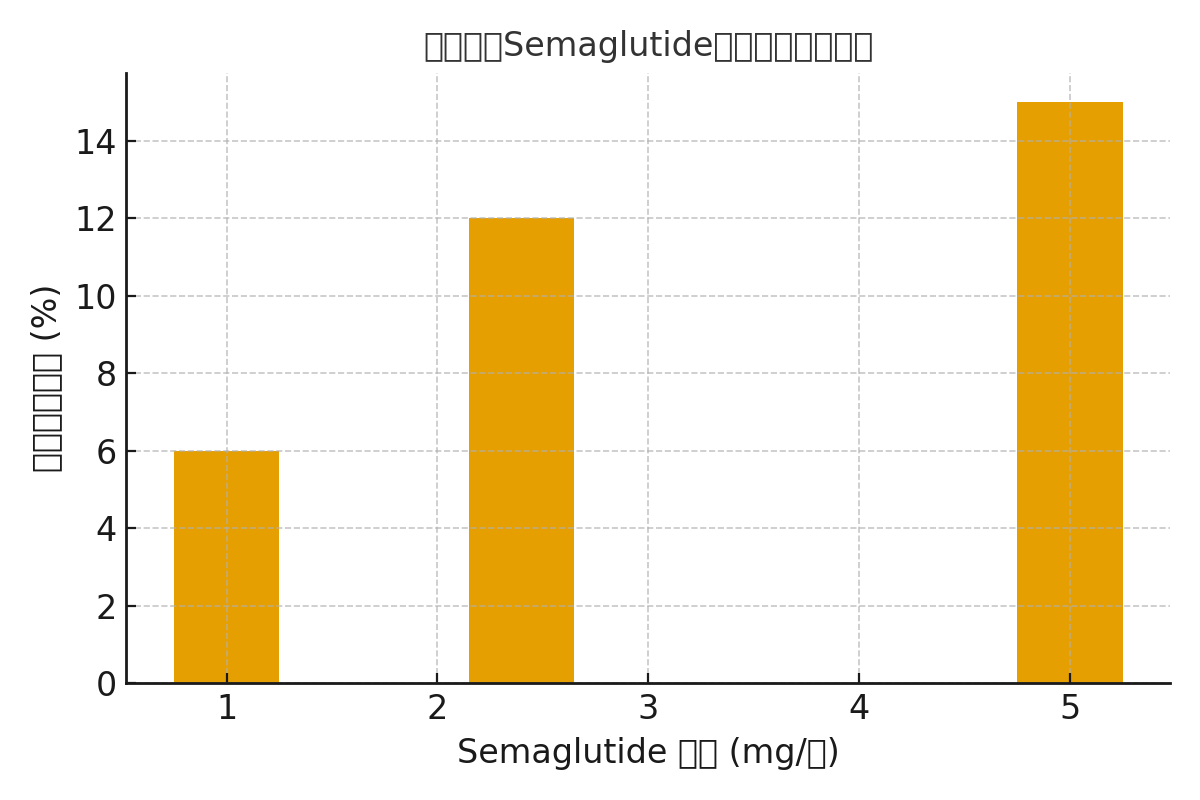
Δοσοεξαρτώμενη επίδρασηΑπό 1mg σε 5mg, η απώλεια βάρους αυξήθηκε προοδευτικά.
-
Βέλτιστη ισορροπίαΗ δόση των 2,4 mg/εβδομάδα έδειξε σημαντικό αποτέλεσμα απώλειας βάρους (12%) και είχε τη μεγαλύτερη ομάδα συμμετεχόντων, γεγονός που υποδηλώνει ότι μπορεί να είναι η πιο συχνά συνιστώμενη δόση στην κλινική πράξη.
-
Ασφάλεια υψηλής δόσηςΗ δόση των 5 mg δεν προκάλεσε σοβαρές ανεπιθύμητες ενέργειες, γεγονός που υποδηλώνει ότι υψηλότερες δόσεις ενδέχεται να ενισχύσουν περαιτέρω την αποτελεσματικότητα υπό ελεγχόμενες συνθήκες ασφαλείας.
Διάγραμμα τάσεων
Το ακόλουθο σχήμα απεικονίζει την επίδραση διαφορετικών δόσεων Σεμαγλουτίδης στη μείωση βάρους:
Σύναψη
Ως καινοτόμο φάρμακο για την απώλεια βάρους, η Σεμαγλουτίδη επιδεικνύει σαφήδοσοεξαρτώμενη επίδραση μείωσης βάρουςσε κλινικές δοκιμές. Με την αύξηση των δόσεων, οι ασθενείς παρουσίασαν μεγαλύτερη μέση απώλεια βάρους. Στο μέλλον, η σεμαγλουτίδη αναμένεται να αποτελέσει ακρογωνιαίο λίθο στη θεραπεία της παχυσαρκίας, παρέχοντας στους κλινικούς ιατρούς περισσότερες επιλογές για εξατομικευμένη θεραπεία.
Ώρα δημοσίευσης: 17 Σεπτεμβρίου 2025