Ιστορικό και Σχεδιασμός Μελέτης
Η ρετατρουτίδη (LY3437943) είναι ένα νέο μονοπεπτιδικό φάρμακο που ενεργοποιείτρεις υποδοχείς ταυτόχρονα: GIP, GLP-1 και γλυκαγόνη. Για την αξιολόγηση της αποτελεσματικότητας και της ασφάλειάς του σε άτομα με παχυσαρκία αλλά χωρίς διαβήτη, διεξήχθη μια τυχαιοποιημένη, διπλά τυφλή, ελεγχόμενη με εικονικό φάρμακο δοκιμή φάσης 2 (NCT04881760). Συνολικά338 συμμετέχοντεςμε ΔΜΣ ≥30 ή ≥27 με τουλάχιστον μία συννοσηρότητα σχετιζόμενη με το βάρος, τυχαιοποιήθηκαν για να λάβουν εικονικό φάρμακο ή ρετατρουτίδη (1 mg, 4 mg με δύο σχήματα τιτλοποίησης, 8 mg με δύο σχήματα τιτλοποίησης ή 12 mg) χορηγούμενη μία φορά την εβδομάδα με υποδόρια ένεση για 48 εβδομάδες.πρωτεύον τελικό σημείοήταν η ποσοστιαία μεταβολή στο σωματικό βάρος στις 24 εβδομάδες, με δευτερεύοντα καταληκτικά σημεία που περιελάμβαναν την μεταβολή βάρους στις 48 εβδομάδες και κατηγορικά όρια απώλειας βάρους (≥5%, ≥10%, ≥15%).
Βασικά Αποτελέσματα
-
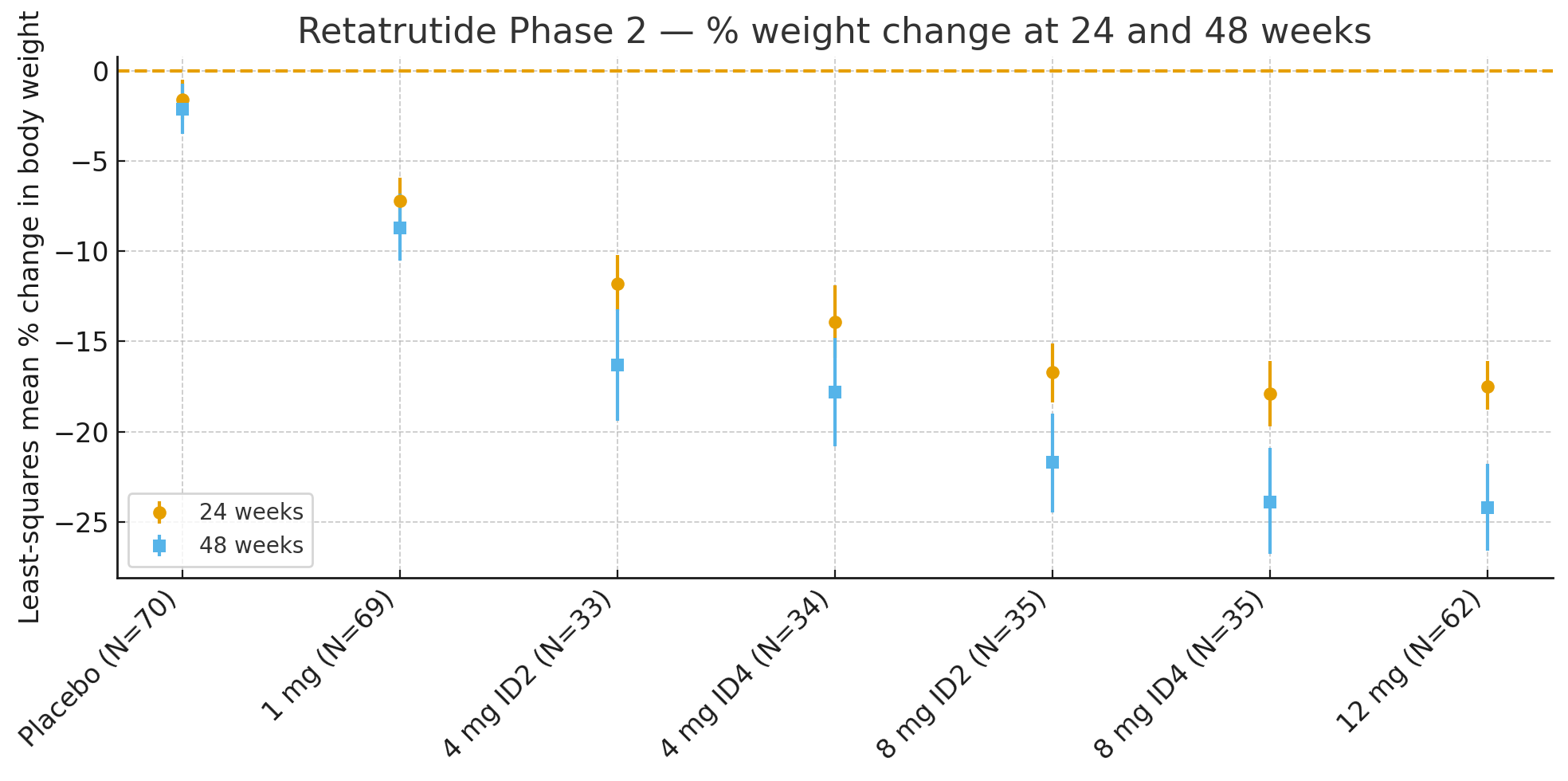
24 εβδομάδεςΗ μέση ποσοστιαία μεταβολή του σωματικού βάρους σε σχέση με την αρχική τιμή ήταν με βάση τα ελαχίστα τετραγώνα
-
Εικονικό φάρμακο: −1,6%
-
1 mg: −7,2%
-
4 mg (συνδυασμένο): −12,9%
-
8 mg (συνδυασμένο): −17,3%
-
12 mg: −17,5%
-
-
48 εβδομάδες: Η ποσοστιαία μεταβολή στο σωματικό βάρος ήταν
-
Εικονικό φάρμακο: −2,1%
-
1 mg: −8,7%
-
4 mg (συνδυασμένο): −17,1%
-
8 mg (συνδυασμένο): −22,8%
-
12 mg: −24,2%
-
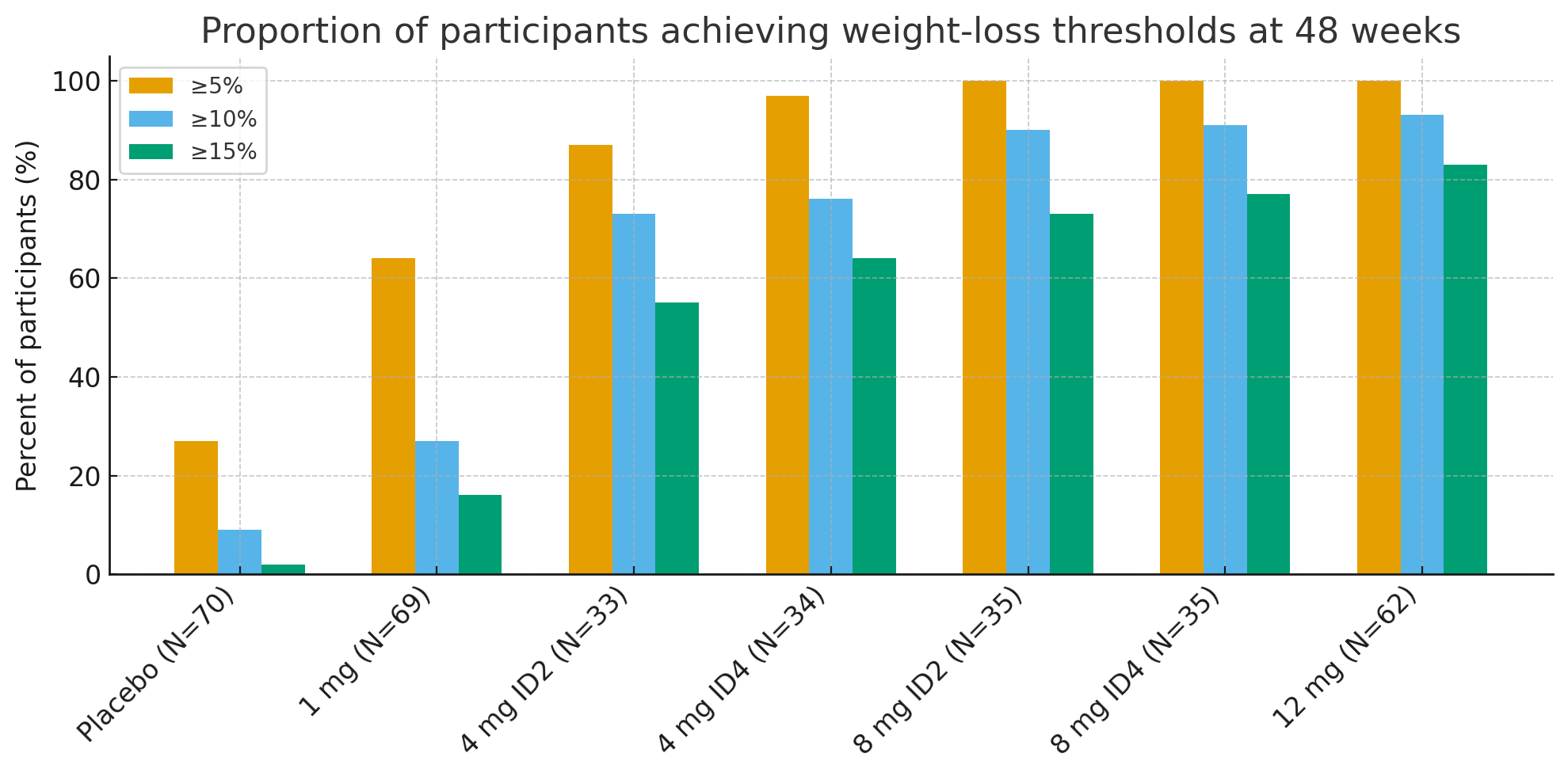
Στις 48 εβδομάδες, τα ποσοστά των συμμετεχόντων που πέτυχαν κλινικά σημαντικά όρια απώλειας βάρους ήταν εντυπωσιακά:
-
Απώλεια βάρους ≥5%: 27% με εικονικό φάρμακο έναντι 92–100% στις ομάδες με ενεργή δράση
-
≥10%: 9% με εικονικό φάρμακο έναντι 73–93% στις ομάδες με δραστική δράση
-
≥15%: 2% με εικονικό φάρμακο έναντι 55–83% στις ομάδες με δραστική δράση
Στην ομάδα των 12 mg, έωςΤο 26% των συμμετεχόντων έχασε ≥30% του αρχικού βάρους τους, ένα μέγεθος απώλειας βάρους συγκρίσιμο με τη βαριατρική χειρουργική επέμβαση.
Ασφάλεια
Οι πιο συχνές ανεπιθύμητες ενέργειες ήταν γαστρεντερικές (ναυτία, έμετος, διάρροια), γενικά ήπιες έως μέτριες και δοσοεξαρτώμενες. Χαμηλότερες αρχικές δόσεις (τιτλοποίηση 2 mg) μείωσαν αυτά τα συμβάντα. Παρατηρήθηκαν δοσοεξαρτώμενες αυξήσεις στον καρδιακό ρυθμό, οι οποίες κορυφώθηκαν την εβδομάδα 24 και στη συνέχεια μειώθηκαν. Τα ποσοστά διακοπής κυμαίνονταν από 6-16% στις δραστικές ομάδες, κάπως υψηλότερα από το εικονικό φάρμακο.
Συμπεράσματα
Σε ενήλικες με παχυσαρκία χωρίς διαβήτη, η εβδομαδιαία υποδόρια χορήγηση ρετατρουτίδης για 48 εβδομάδες παρήγαγεσημαντικές, δοσοεξαρτώμενες μειώσεις στο σωματικό βάρος(έως ~24% μέση απώλεια στην υψηλότερη δόση), μαζί με βελτιώσεις στους καρδιομεταβολικούς δείκτες. Οι γαστρεντερικές ανεπιθύμητες ενέργειες ήταν συχνές αλλά αντιμετωπίσιμες με τιτλοποίηση. Αυτά τα ευρήματα φάσης 2 υποδηλώνουν ότι η ρετατρουτίδη θα μπορούσε να αποτελέσει ένα νέο θεραπευτικό σημείο αναφοράς για την παχυσαρκία, εν αναμονή επιβεβαίωσης σε μεγαλύτερες, μακροπρόθεσμες δοκιμές φάσης 3.
Ώρα δημοσίευσης: 28 Σεπτεμβρίου 2025