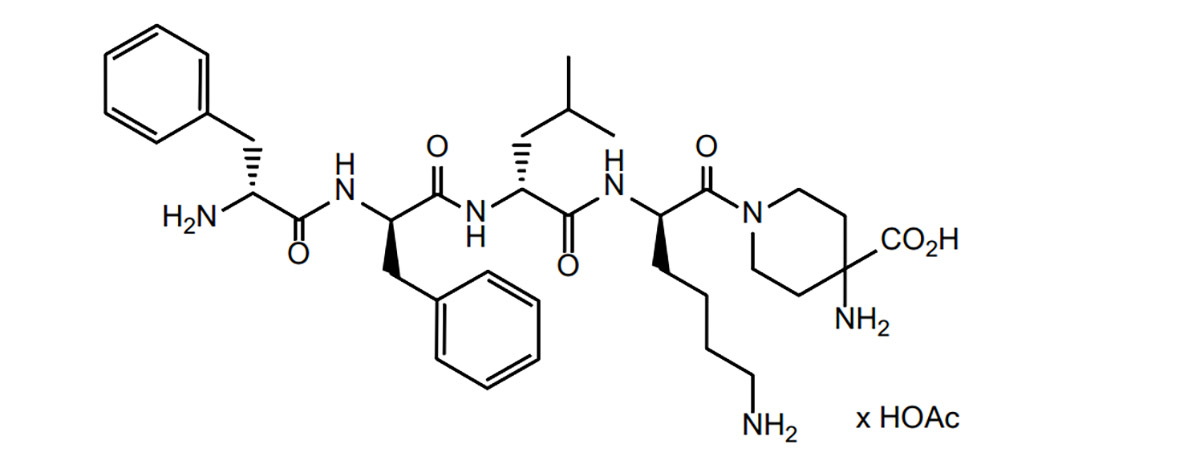
Ήδη στις 24-08-2021, η Cara Therapeutics και ο επιχειρηματικός της συνεργάτης Vifor Pharma ανακοίνωσαν ότι ο πρώτος στην κατηγορία του αγωνιστής υποδοχέα κάππα οπιοειδών, διφελικεφαλίνη (KORSUVA™), εγκρίθηκε από τον FDA για τη θεραπεία ασθενών με χρόνια νεφρική νόσο (ΧΝΝ) (θετικός μέτριος/σοβαρός κνησμός με αιμοκάθαρση) και αναμένεται να κυκλοφορήσει το πρώτο τρίμηνο του 2022. Η Cara και η Vifor υπέγραψαν αποκλειστική συμφωνία άδειας χρήσης για την εμπορευματοποίηση του KORSUVA™ στις Ηνωμένες Πολιτείες και συμφώνησαν να πουλήσουν το KORSUVA™ στην Fresenius Medical. Μεταξύ αυτών, η Cara και η Vifor έχουν μερίδιο κέρδους 60% και 40% στα έσοδα από πωλήσεις, εκτός από την Fresenius Medical. Η καθεμία έχει μερίδιο κέρδους 50% στα έσοδα από πωλήσεις από την Fresenius Medical.
Ο κνησμός που σχετίζεται με τη ΧΝΝ (CKD-aP) είναι ένας γενικευμένος κνησμός που εμφανίζεται με υψηλή συχνότητα και ένταση σε ασθενείς με ΧΝΝ που υποβάλλονται σε αιμοκάθαρση. Ο κνησμός εμφανίζεται σε περίπου 60%-70% των ασθενών που υποβάλλονται σε αιμοκάθαρση, εκ των οποίων το 30%-40% έχει μέτριο/σοβαρό κνησμό, ο οποίος επηρεάζει σοβαρά την ποιότητα ζωής (π.χ. κακή ποιότητα ύπνου) και σχετίζεται με κατάθλιψη. Δεν υπάρχει αποτελεσματική θεραπεία για τον κνησμό που σχετίζεται με τη ΧΝΝ μέχρι σήμερα και η έγκριση του Difelikefalin βοηθά στην αντιμετώπιση του τεράστιου κενού στις ιατρικές ανάγκες. Αυτή η έγκριση βασίζεται σε δύο βασικές κλινικές δοκιμές Φάσης III που έχουν κατατεθεί για την NDA: θετικά δεδομένα από τις δοκιμές KALM-1 και KALM-2 στις ΗΠΑ και παγκοσμίως, και υποστηρικτικά δεδομένα από 32 επιπλέον κλινικές μελέτες, τα οποία καταδεικνύουν ότι το KORSUVA™ είναι καλά ανεκτό.
Πριν από λίγο καιρό, ήρθαν καλά νέα από την κλινική μελέτη της διφελικεφαλίνης στην Ιαπωνία: 2022-10-1, η Cara ανακοίνωσε ότι οι συνεργάτες της, Maruishi Pharma και Kissey Pharma, επιβεβαίωσαν ότι η ένεση διφελικεφαλίνης χρησιμοποιείται στην Ιαπωνία για τη θεραπεία του κνησμού σε ασθενείς που υποβάλλονται σε αιμοκάθαρση. Κλινικές δοκιμές Φάσης III. Το κύριο καταληκτικό σημείο επιτεύχθηκε. 178 ασθενείς έλαβαν 6 εβδομάδες διφελικεφαλίνης ή εικονικού φαρμάκου και συμμετείχαν σε μια ανοιχτή μελέτη επέκτασης 52 εβδομάδων. Το κύριο καταληκτικό σημείο (αλλαγή στη βαθμολογία της κλίμακας αριθμητικής αξιολόγησης του κνησμού) και το δευτερεύον καταληκτικό σημείο (αλλαγή στη βαθμολογία του κνησμού στην κλίμακα σοβαρότητας Shiratori) βελτιώθηκαν σημαντικά από την αρχική τιμή στην ομάδα της διφελικεφαλίνης σε σύγκριση με την ομάδα του εικονικού φαρμάκου και ήταν καλά ανεκτά.
Η διφελικεφαλίνη είναι μια κατηγορία οπιοειδών πεπτιδίων. Με βάση αυτό, το Ινστιτούτο Έρευνας Πεπτιδίων μελέτησε τη βιβλιογραφία για τα οπιοειδή πεπτίδια και συνόψισε τις δυσκολίες και τις στρατηγικές των οπιοειδών πεπτιδίων στην ανάπτυξη φαρμάκων, καθώς και την τρέχουσα κατάσταση ανάπτυξης φαρμάκων.
Ώρα δημοσίευσης: 17 Φεβρουαρίου 2022